


Le tableau périodique est une disposition tabulaire des éléments chimiques, organisée en fonction de leur numéro atomique, de leur configuration électronique et de leurs propriétés chimiques. Les éléments sont disposés en lignes (appelées périodes) et en colonnes (appelées groupes ou familles) dans l'ordre croissant de leur numéro atomique.
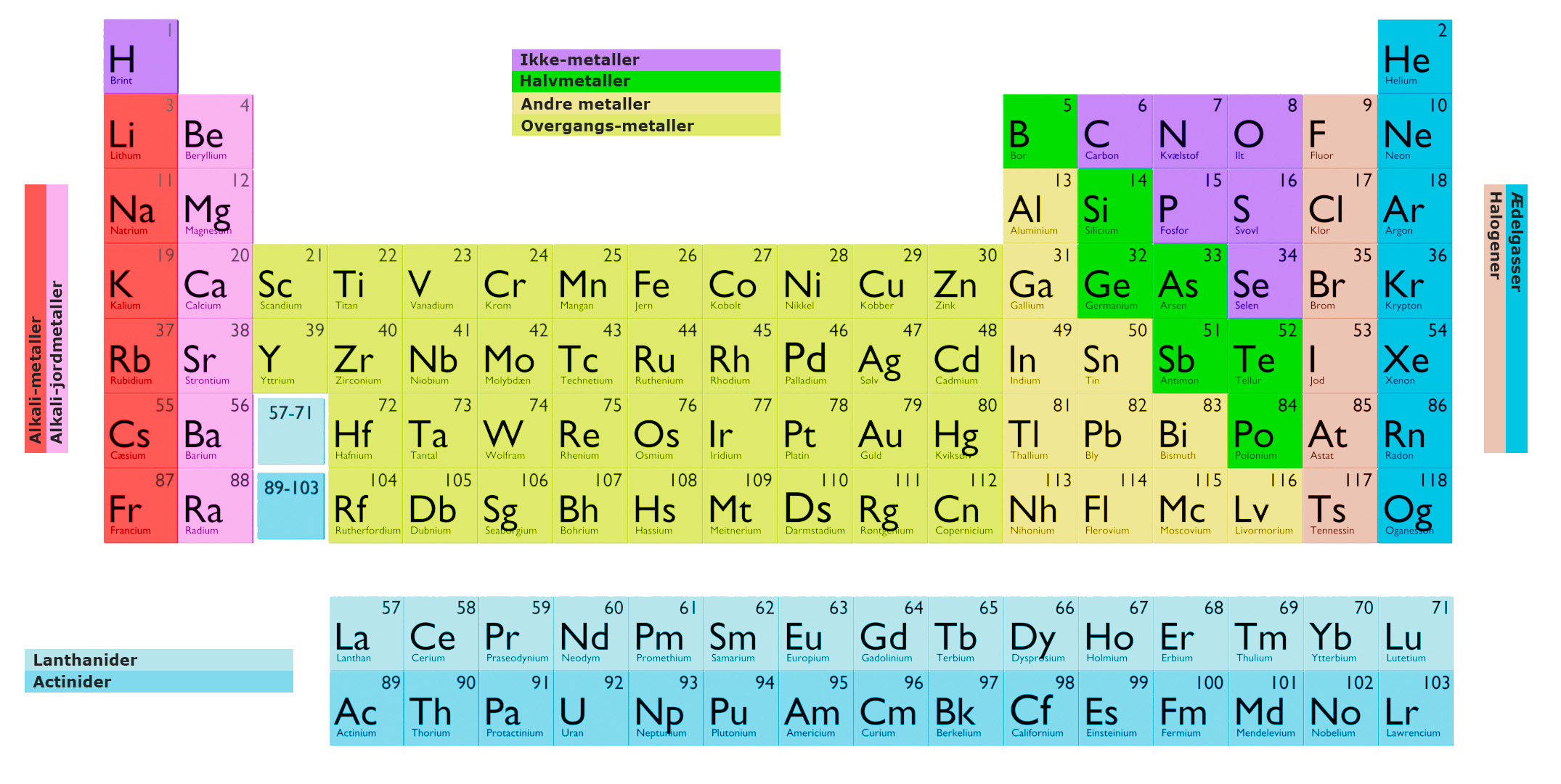
Chaque élément est représenté par un symbole chimique unique, généralement une ou deux lettres, utilisé pour l'identifier dans le tableau périodique. Les éléments sont également regroupés en catégories selon leurs propriétés physiques et chimiques.
Les éléments de la première colonne (appelée groupe 1) sont appelés métaux alcalins et possèdent des propriétés similaires. Les éléments de la deuxième colonne (groupe 2) sont appelés métaux alcalino-terreux et ont des propriétés similaires. Les éléments des six colonnes suivantes (groupes 3 à 8) sont appelés métaux de transition et présentent des propriétés similaires. Les éléments de la dernière colonne (groupe 18) sont appelés gaz nobles et ont des propriétés similaires.
Les lignes du tableau périodique sont appelées périodes. La première ligne (période 1) ne comporte que deux éléments, l'hydrogène et l'hélium. Les lignes suivantes contiennent chacune 8 éléments, de la période 2 à la période 7.
Les éléments d'une même période ont des configurations électroniques similaires, mais lorsqu'on se déplace de la gauche vers la droite à travers une période, le numéro atomique augmente, ce qui entraîne une augmentation du nombre de protons dans le noyau, ce qui conduit à une augmentation du nombre d'électrons dans la couche externe, ce qui entraîne différentes propriétés chimiques et physiques.
Les éléments d'un même groupe (ou colonne) ont des propriétés chimiques similaires, car ils possèdent le même nombre d'électrons dans leur couche externe.
Le tableau périodique est un outil efficace pour prédire les propriétés et le comportement des éléments et de leurs composés, et il est largement utilisé en chimie et dans d'autres sciences.
Les métaux alcalins sont un groupe d'éléments du tableau périodique situés dans le groupe 1 (IA). Ils se caractérisent par la présence d'un seul électron de valence dans leur couche externe. Ils ont des propriétés chimiques et physiques similaires, et ils sont très réactifs. Les métaux alcalins sont :
| Élément | Description |
|---|---|
| Lithium (Li) | Le métal alcalin le plus léger et le moins réactif. Il est utilisé dans les batteries et d'autres applications. |
| Sodium (Na) | Le métal alcalin le plus courant, utilisé dans de nombreux procédés industriels, y compris la production de verre, de savon et de produits chimiques. |
| Potassium (K) | Utilisé dans les engrais, les feux d'artifice et d'autres applications. |
| Rubidium (Rb) | Moins courant et utilisé dans des applications spécialisées, telles que les horloges atomiques et la recherche. |
| Césium (Cs) | N'est pas non plus couramment utilisé. |
| Francium (Fr) | Le métal alcalin le plus rare et le plus instable, que l'on ne trouve qu'en très petites quantités dans la nature. |
Les métaux alcalino-terreux sont un groupe d'éléments du tableau périodique situés dans le groupe 2 (IIA). Ils se caractérisent par la présence de deux électrons de valence dans leur couche externe. Ils ont des propriétés chimiques et physiques similaires, et ils sont moins réactifs que les métaux alcalins. Les métaux alcalino-terreux sont :
| Élément | Description |
|---|---|
| Béryllium (Be) | Un métal léger et résistant avec des propriétés uniques qui le rendent utile dans l'aéronautique, l'énergie nucléaire et d'autres applications de haute technologie. |
| Magnésium (Mg) | Utilisé dans les alliages, les feux d'artifice et comme cathode dans les batteries. |
| Calcium (Ca) | Un élément essentiel pour les organismes vivants et le métal le plus abondant dans le corps humain. Il est utilisé dans l'industrie du bâtiment pour la fabrication du ciment et de la chaux. |
| Strontium (Sr) | Utilisé dans les fusées de détresse, les feux d'artifice et comme source de strontium-90, un isotope radioactif utilisé dans les traitements médicaux. |
| Baryum (Ba) | Utilisé dans l'industrie pétrolière et gazière, ainsi que dans la production de verre et de céramique. |
| Radium (Ra) | Radioactif et ne se trouve qu'en petites quantités dans la nature, il n'a aucune application commerciale. |
Les métaux de transition sont un groupe d'éléments du tableau périodique situés dans les groupes 3 à 12 (IIIB-IIB) et comprennent les séries des lanthanides et des actinides. Ils se caractérisent par la présence d'orbitales d partiellement remplies dans leur couche externe.
Ils présentent diverses propriétés chimiques et physiques et sont connus pour leurs points de fusion et d'ébullition élevés ainsi que pour leur densité élevée. Ils sont également connus pour leur capacité à former plusieurs états d'oxydation et pour leurs composés colorés. Quelques-uns des métaux de transition courants sont :
| Élément | Description |
|---|---|
| Scandium (Sc) | |
| Vanadium (V) | |
| Chrome (Cr) | |
| Manganèse (Mn) | |
| Fer (Fe) | |
| Cobalt (Co) | |
| Nickel (Ni) | |
| Cuivre (Cu) | |
| Zinc (Zn) | |
| Molybdène (Mo) | |
| Ruthénium (Ru) | |
| Rhodium (Rh) | |
| Palladium (Pd) | |
| Argent (Ag) | |
| Cadmium (Cd) | |
| Mercure (Hg) | |
| Platine (Pt) | |
| Or (Au) |
| Élément | Description |
|---|---|
| Hélium (He) | Le deuxième élément le plus léger et utilisé dans les ballons, les dirigeables et comme fluide de refroidissement pour la cryogénie. |
| Néon (Ne) | Utilisé dans les enseignes lumineuses, les tubes cathodiques et comme fluide de refroidissement pour la cryogénie. |
| Argon (Ar) | Utilisé dans les ampoules, le soudage et comme gaz inerte dans les laboratoires. |
| Krypton (Kr) | Utilisé dans les lampes flash, les stroboscopes et comme fluide de refroidissement pour la cryogénie. |
| Xénon (Xe) | Comme le krypton, utilisé dans les lampes flash, les stroboscopes et comme fluide de refroidissement pour la cryogénie. |
| Radon (Rn) | C'est un gaz radioactif et il n'est pas utilisé commercialement. |
Ces gaz sont considérés comme chimiquement inertes, ce qui signifie qu'ils ne participent pas aux réactions chimiques et, par conséquent, ne forment pas de composés. Cependant, ils peuvent être forcés à réagir sous haute pression ou à des températures extrêmes.
