


Das Periodensystem ist eine tabellarische Anordnung der chemischen Elemente, organisiert nach ihrer Ordnungszahl, Elektronenkonfiguration und chemischen Eigenschaften. Die Elemente sind in Reihen (genannt Perioden) und Spalten (genannt Gruppen oder Familien) in aufsteigender Reihenfolge der Ordnungszahl angeordnet.
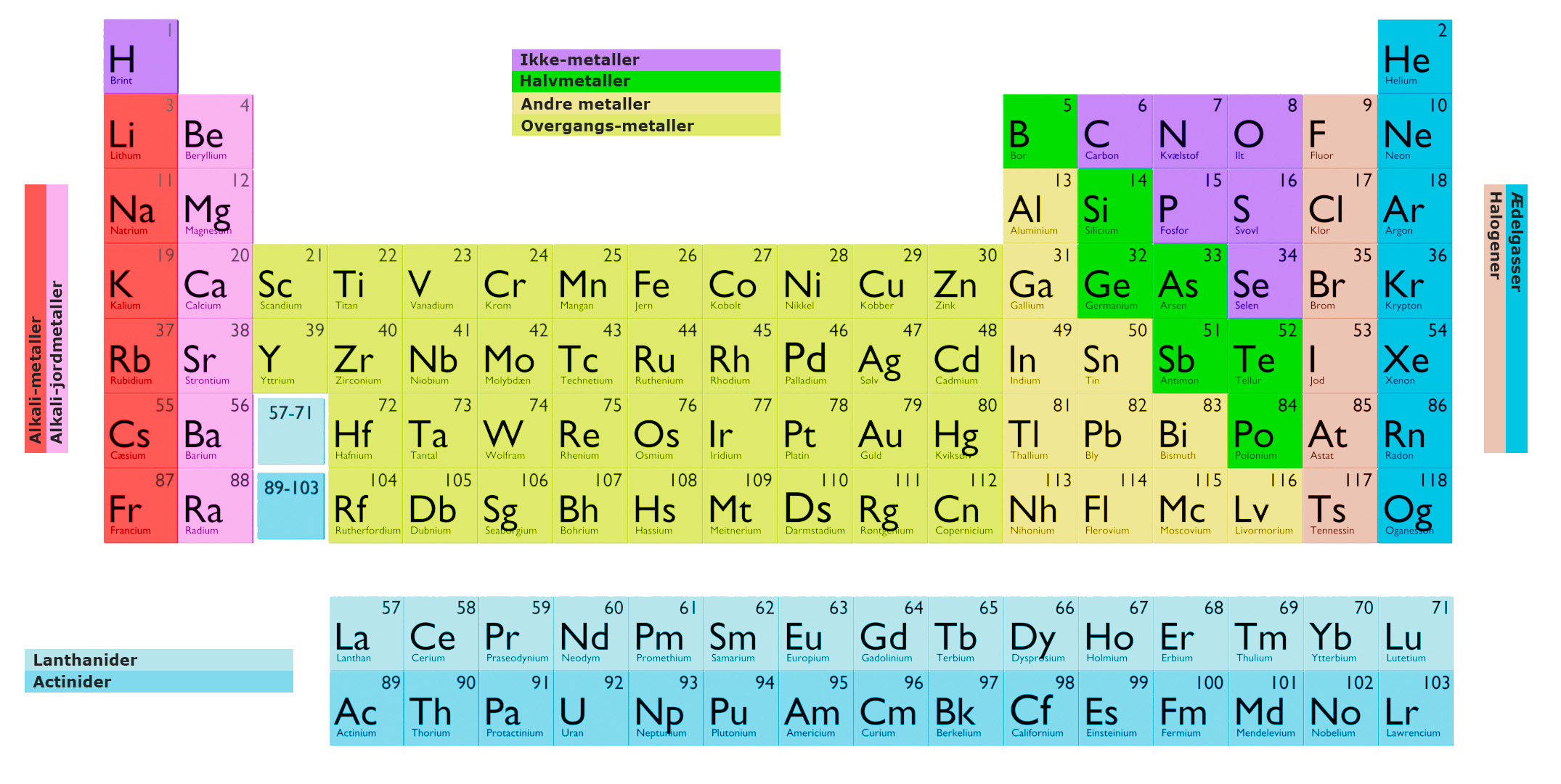
Jedes Element wird durch ein einzigartiges chemisches Symbol dargestellt, typischerweise ein oder zwei Buchstaben, die zur Identifizierung im Periodensystem verwendet werden. Die Elemente werden auch in Kategorien gruppiert, basierend auf ihren physikalischen und chemischen Eigenschaften.
Die Elemente in der ersten Spalte (genannt Gruppe 1) werden Alkalimetalle genannt und haben ähnliche Eigenschaften. Die Elemente in der zweiten Spalte (Gruppe 2) werden Erdalkalimetalle genannt und haben ähnliche Eigenschaften. Die Elemente in den nächsten sechs Spalten (Gruppen 3-8) werden Übergangsmetalle genannt und haben ähnliche Eigenschaften. Die Elemente in der letzten Spalte (Gruppe 18) werden Edelgase genannt und haben ähnliche Eigenschaften.
Die Reihen im Periodensystem werden Perioden genannt. Die erste Reihe (Periode 1) hat nur zwei Elemente, Wasserstoff und Helium. Die nächsten Reihen haben jeweils 8 Elemente, von Periode 2 bis Periode 7.
Die Elemente in derselben Periode haben ähnliche Elektronenkonfigurationen, aber wenn man sich von links nach rechts über eine Periode bewegt, steigt die Ordnungszahl, was zu einer Zunahme der Protonenzahl im Kern führt, was wiederum zu einer Zunahme der Elektronenzahl in der äußersten Schale führt, was zu unterschiedlichen chemischen und physikalischen Eigenschaften führt.
Die Elemente in derselben Gruppe (oder Spalte) haben ähnliche chemische Eigenschaften, weil sie die gleiche Anzahl an Elektronen in ihrer äußersten Schale haben.
Das Periodensystem ist ein effektives Werkzeug zur Vorhersage von Eigenschaften und Verhalten von Elementen und deren Verbindungen und wird häufig in der Chemie und anderen Wissenschaften verwendet.
Die Alkalimetalle sind eine Gruppe von Elementen im Periodensystem, die in Gruppe 1 (IA) angeordnet sind. Sie zeichnen sich dadurch aus, dass sie ein Valenzelektron in ihrer äußersten Schale besitzen. Sie haben ähnliche chemische und physikalische Eigenschaften und sind sehr reaktiv. Die Alkalimetalle sind:
| Element | Beschreibung |
|---|---|
| Lithium (Li) | Das leichteste Alkalimetall und das am wenigsten reaktive. Es wird in Batterien und anderen Anwendungen verwendet. |
| Natrium (Na) | Das am häufigsten vorkommende Alkalimetall, das in vielen industriellen Prozessen verwendet wird, einschließlich der Herstellung von Glas, Seife und Chemikalien |
| Kalium (K) | Wird in Düngemitteln, Feuerwerk und anderen Anwendungen verwendet |
| Rubidium (Rb) | Weniger verbreitet und wird in spezialisierten Anwendungen wie Atomuhren und Forschung verwendet |
| Caesium (Cs) | Wird ebenfalls nicht häufig verwendet |
| Francium (Fr) | Das seltenste und instabilste Alkalimetall und kommt nur in kleinen Mengen in der Natur vor |
Die Erdalkalimetalle sind eine Gruppe von Elementen im Periodensystem, die in Gruppe 2 (IIA) angeordnet sind. Sie zeichnen sich dadurch aus, dass sie zwei Valenzelektronen in ihrer äußersten Schale besitzen. Sie haben ähnliche chemische und physikalische Eigenschaften und sind weniger reaktiv als die Alkalimetalle. Die Erdalkalimetalle bestehen aus:
| Element | Beschreibung |
|---|---|
| Beryllium (Be) | Ein leichtes und starkes Metall mit einzigartigen Eigenschaften, das es für die Luftfahrt, Kernenergie und andere Hightech-Anwendungen nützlich macht |
| Magnesium (Mg) | Wird in Legierungen, Feuerwerk und als Kathode in Batterien verwendet |
| Calcium (Ca) | Ein essentielles Element für lebende Organismen und das am häufigsten vorkommende Metall im menschlichen Körper. Es wird in der Bauindustrie zur Herstellung von Zement und Kalk verwendet |
| Strontium (Sr) | Wird in Leuchtraketen, Feuerwerk und als Quelle für Strontium-90, ein radioaktives Isotop, das in medizinischen Behandlungen verwendet wird, eingesetzt. |
| Barium (Ba) | Wird in der Öl- und Gasindustrie sowie bei der Herstellung von Glas und Keramik verwendet |
| Radium (Ra) | Radioaktiv und kommt nur in kleinen Mengen in der Natur vor und hat keine kommerzielle Anwendung |
Die Übergangsmetalle sind eine Gruppe von Elementen im Periodensystem, die in den Gruppen 3-12 (IIIB-IIB) angeordnet sind und die Lanthanoid- und Actinoidreihe umfassen. Sie zeichnen sich dadurch aus, dass sie teilweise gefüllte d-Orbitale in ihrer äußersten Schale besitzen.
Sie haben unterschiedliche chemische und physikalische Eigenschaften und sind bekannt für ihre hohen Schmelz- und Siedepunkte sowie hohe Dichten. Sie sind auch bekannt für ihre Fähigkeit, mehrere Oxidationsstufen zu bilden und für ihre farbigen Verbindungen. Einige der häufigen Übergangsmetalle sind:
| Element | Beschreibung |
|---|---|
| Scandium (Sc) | |
| Vanadium (V) | |
| Chrom (Cr) | |
| Mangan (Mn) | |
| Eisen (Fe) | |
| Kobalt (Co) | |
| Nickel (Ni) | |
| Kupfer (Cu) | |
| Zink (Zn) | |
| Molybdän (Mo) | |
| Ruthenium (Ru) | |
| Rhodium (Rh) | |
| Palladium (Pd) | |
| Silber (Ag) | |
| Cadmium (Cd) | |
| Quecksilber (Hg) | |
| Platin (Pt) | |
| Gold (Au) |
| Element | Beschreibung |
|---|---|
| Helium (He) | Das zweitleichteste Element und wird in Ballons, Luftschiffen und als Kühlmittel für Kryotechnik verwendet |
| Neon (Ne) | Wird in Leuchtreklamen, Fernsehbildröhren und als Kühlmittel für Kryotechnik verwendet |
| Argon (Ar) | Wird in Glühbirnen, beim Schweißen und als Inertgas in Laboratorien verwendet |
| Krypton (Kr) | Wird in Blitzlampen, Stroboskoplichtern und als Kühlmittel für Kryotechnik verwendet |
| Xenon (Xe) | Wie Krypton wird es in Blitzlampen, Stroboskoplichtern und als Kühlmittel für Kryotechnik verwendet |
| Radon (Rn) | Ist ein radioaktives Gas und wird nicht kommerziell verwendet |
Diese Gase gelten als chemisch inert, was bedeutet, dass sie nicht an chemischen Reaktionen teilnehmen und daher keine Verbindungen bilden. Sie können jedoch unter hohem Druck oder extremen Temperaturen zur Reaktion gezwungen werden.
