


La tabla periódica es una disposición en forma de tabla de los elementos químicos, organizada en base a su número atómico, configuraciones electrónicas y propiedades químicas. Los elementos están organizados en filas (llamadas períodos) y columnas (llamadas grupos o familias) en orden de número atómico creciente.
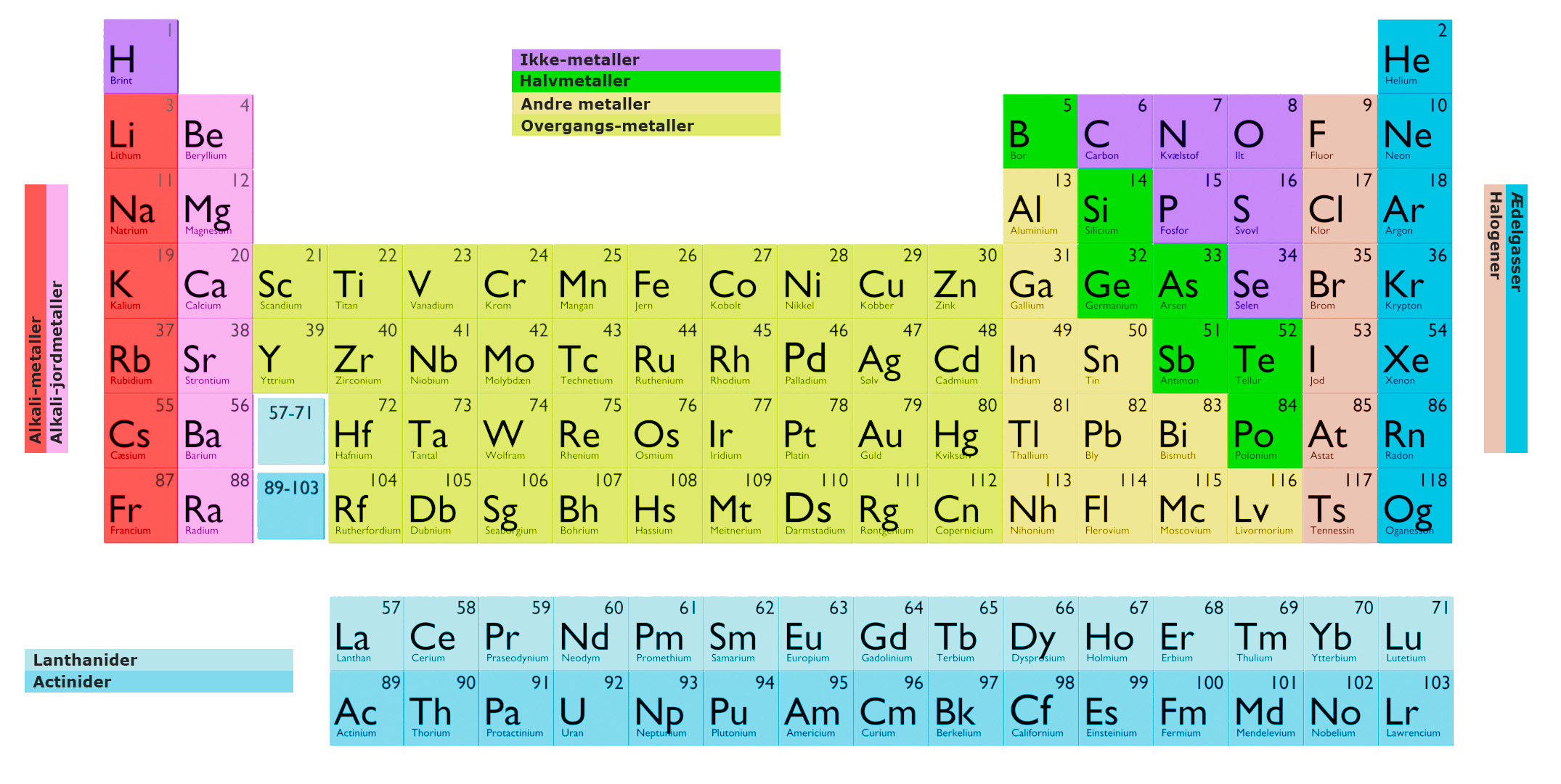
Cada elemento está representado por un símbolo químico único, normalmente una o dos letras, que se utiliza para identificarlo en la tabla periódica. Los elementos también se agrupan en categorías basadas en sus propiedades físicas y químicas.
Los elementos en la primera columna (llamada grupo 1) se llaman metales alcalinos y tienen propiedades similares. Los elementos en la segunda columna (grupo 2) se llaman metales alcalinotérreos y tienen propiedades similares. Los elementos en las siguientes seis columnas (grupos 3-8) se llaman metales de transición y tienen propiedades similares. Los elementos en la última columna (grupo 18) se llaman gases nobles y tienen propiedades similares.
Las filas de la tabla periódica se llaman períodos. La primera fila (período 1) tiene solo dos elementos, hidrógeno y helio. Las siguientes filas tienen 8 elementos cada una, desde el período 2 hasta el período 7.
Los elementos en el mismo período tienen configuraciones electrónicas similares, pero al moverse de izquierda a derecha a lo largo de un período, el número atómico aumenta, lo que lleva a un aumento en el número de protones en el núcleo, lo que a su vez lleva a un aumento en el número de electrones en la capa más externa, lo que conduce a diferentes propiedades químicas y físicas.
Los elementos en el mismo grupo (o columna) tienen propiedades químicas similares porque tienen el mismo número de electrones en su capa más externa.
La tabla periódica es una herramienta eficaz para predecir las propiedades y el comportamiento de los elementos y sus compuestos, y se utiliza ampliamente en la química y otras ciencias.
Los metales alcalinos son un grupo de elementos en la tabla periódica que se encuentran en el grupo 1 (IA). Se caracterizan por tener un electrón de valencia en su capa más externa. Tienen propiedades químicas y físicas similares, y son muy reactivos. Los metales alcalinos son:
| Elemento | Descripción |
|---|---|
| Lithium (Li) | El metal alcalino más ligero y el menos reactivo. Se utiliza en baterías y otras aplicaciones. |
| Sodium (Na) | El metal alcalino más común, utilizado en muchos procesos industriales, incluyendo la producción de vidrio, jabón y productos químicos |
| Potassium (K) | Se utiliza en fertilizantes, fuegos artificiales y otras aplicaciones |
| Rubidium (Rb) | Menos común y se utiliza en aplicaciones especializadas, como relojes atómicos e investigación |
| Cesium (Cs) | Tampoco es de uso común |
| Francium (Fr) | El metal alcalino más raro y más inestable, y solo se encuentra en pequeñas cantidades en la naturaleza |
Los metales alcalinotérreos son un grupo de elementos en la tabla periódica que se encuentran en el grupo 2 (IIA). Se caracterizan por tener dos electrones de valencia en su capa más externa. Tienen propiedades químicas y físicas similares, y son menos reactivos que los metales alcalinos. Los metales alcalinotérreos consisten en:
| Elemento | Descripción |
|---|---|
| Beryllium (Be) | Un metal ligero y fuerte con propiedades únicas que lo hacen útil en la industria aeroespacial, energía nuclear y otras aplicaciones de alta tecnología |
| Magnesium (Mg) | Se utiliza en aleaciones, fuegos artificiales y como cátodo en baterías |
| Calcium (Ca) | Un elemento esencial para los seres vivos y el metal más abundante en el cuerpo humano. Se utiliza en la industria de la construcción para la fabricación de cemento y cal |
| Strontium (Sr) | Se utiliza en bengalas, fuegos artificiales y como fuente de estroncio-90, un isótopo radiactivo utilizado en tratamientos médicos. |
| Barium (Ba) | Se utiliza en la industria del petróleo y gas, y en la producción de vidrio y cerámica |
| Radium (Ra) | Radiactivo y solo se encuentra en pequeñas cantidades en la naturaleza y no tiene aplicación comercial |
Los metales de transición son un grupo de elementos en la tabla periódica que se encuentran en los grupos 3-12 (IIIB-IIB) e incluyen las series de lantánidos y actínidos. Se caracterizan por tener orbitales d parcialmente llenos en su capa más externa.
Tienen diversas propiedades químicas y físicas y son conocidos por sus altos puntos de fusión y ebullición, así como por sus altas densidades. También son conocidos por su capacidad para formar varios estados de oxidación y por sus compuestos coloreados. Algunos de los metales de transición más comunes son:
| Elemento | Descripción |
|---|---|
| Scandium (Sc) | |
| Vanadium (V) | |
| Chromium (Cr) | |
| Manganese (Mn) | |
| Iron (Fe) | |
| Cobalt (Co) | |
| Nickel (Ni) | |
| Copper (Cu) | |
| Zinc (Zn) | |
| Molybdenum (Mo) | |
| Ruthenium (Ru) | |
| Rhodium (Rh) | |
| Palladium (Pd) | |
| Silver (Ag) | |
| Cadmium (Cd) | |
| Mercury (Hg) | |
| Platinum (Pt) | |
| Gold (Au) |
| Elemento | Descripción |
|---|---|
| Helium (He) | El segundo elemento más ligero y se utiliza en globos, dirigibles y como refrigerante para criogenia |
| Neon (Ne) | Se utiliza en letreros luminosos, tubos de televisión y como refrigerante para criogenia |
| Argon (Ar) | Se utiliza en bombillas, soldadura y como gas inerte en laboratorios |
| Krypton (Kr) | Se utiliza en flashes, luces estroboscópicas y como refrigerante para criogenia |
| Xenon (Xe) | Como el criptón, se utiliza en flashes, luces estroboscópicas y como refrigerante para criogenia |
| Radon (Rn) | Es un gas radiactivo y no se utiliza comercialmente |
Estos gases se consideran químicamente inertes, lo que significa que no participan en reacciones químicas, y por lo tanto no forman compuestos. Sin embargo, pueden ser forzados a reaccionar bajo alta presión o temperaturas extremas.
